-
4月17日,美国食品和药物管理局批准了 Omisirge (omidubicel-onlv),这是一种经过实质性改良的同种异体(供体)脐带血细胞疗法,可加快体内嗜中性粒细胞(白细胞...
2023-04-25
-
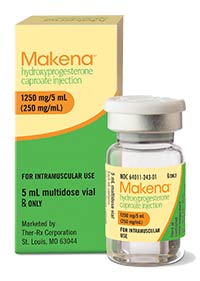
4月6日,美国食品和药物管理局宣布了撤回对Makena的批准,Makena是一种根据加速批准途径获得批准的药物。该药物被批准用于降低有自然早产史的孕妇早产的风险。该决定由FDA专员...
2023-04-10
-
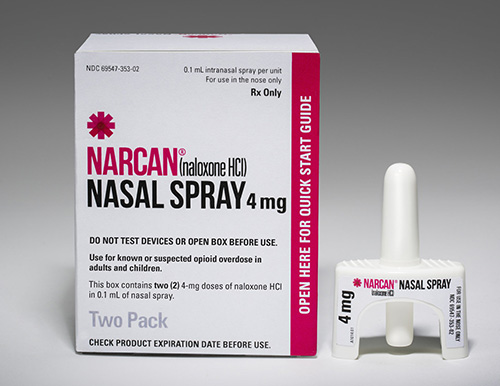
今天,美国食品和药物管理局批准了 Narcan,4 毫克 (mg) 盐酸纳洛酮鼻腔喷雾剂用于非处方药 (OTC)。这是第一个获准在没有处方的情况下使用的纳洛酮产品。纳洛酮是一种可迅...
2023-03-29
-
3月24日,美国食品和药物管理局发布了指南草案,即支持肿瘤治疗加速批准的临床试验注意事项,涉及支持加速批准申请的临床试验设计注意事项。加速批准途径通常用于批准肿瘤药物,部分原因是癌...
2023-03-28
-
EMA的安全委员会(PRAC)已经开始对含有伪麻黄碱的药物进行审查,因为担心后部可逆性脑病综合征(PRES)和可逆性脑血管收缩综合征(RCVS)的风险,这些疾病会影响大脑血管。伪麻...
2023-02-12
-
2023年2月1日,美国食品和药物管理局批准Jesduvroq片剂(daprodustat)为接受透析至少四个月的成年人首次口服治疗慢性肾脏疾病引起的贫血(红细胞数量减少)。Jes...
2023-02-05
-
2023年1月6日,美国食品和药物管理局通过加速批准途径批准了Leqembi(lecanemab-irmb)用于治疗阿尔茨海默病。Leqembi是批准用于阿尔茨海默病的新药物类别中...
2023-02-05
-
2022年12月22日,美国食品和药物管理局批准了(lenacapavir),这是一种新型抗逆转录病毒药物,用于患有人类免疫缺陷病毒1型(HIV-1)的成年患者,由于耐药性,不耐受...
2023-02-05
-
EMA的安全委员会PRAC已经完成了对含有磷酸可定的药物的审查,这些药物用于成人和儿童治疗非生产性(干性)咳嗽,并与其他活性物质联合用于治疗感冒和流感症状,并建议撤销这些药物的欧盟...
2022-12-04
-
11月30日,美国食品和药物管理局批准了,这是该机构批准的第一种粪便微生物群产品。Rebyota 被批准用于预防 18 岁及以上个体艰难梭菌感染 (CDI) 的复发。它适用于个体完...
2022-12-04