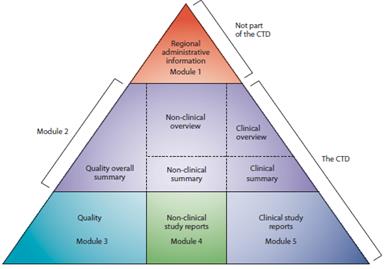
为贯彻落实国务院《关于改革药品医疗器械审评审批制度的意见》(国发〔2015〕44号)的有关要求,加快建立我国药品电子通用技术文档(eCTD)系统,实现2017年年底化学仿制药按eCTD要求实行申报受理,总局药化注册司和我中心在社会各方的支持和帮助下,组织信息、药学、药理毒理、临床、统计和临床药理学等专业审评人员起草了《药品电子通用技术文档结构(征求意见稿)》和《化学仿制药电子通用技术文档申报指导原则(征求意见稿)》,现向社会公开征求意见。请将建议和修改意见于2017年6月30日前通过电子邮件反馈至我中心。
| 下载信息 [文件大小:346 KB 下载次数: 次] |
| 下载信息 [文件大小:1919 KB 下载次数: 次] |
原文链接:http://www.cde.org.cn/news.do?method=viewInfoCommon&id=313618