【新闻事件】:诺华CDK4/6抑制剂ribociclib(LEE011)在一个叫做MONALEESA-2的3期临床试验中,和来曲唑联合使用相比安慰剂对照组因显著延长患者的无进展生存期(PFS)而被提前终止。MONALEESA-2是一项随机、双盲、安慰剂对照的关键3期临床试验,在全球294个中心的668位激素受体阳性(HR+)和人表皮生长因子受体2阴性(HER2-)的绝经后妇女患者中进行。一级实验终点是无进展生存期(PFS),次要终点有总生存期(OS)、客观应答率(ORR)、生活质量、安全性和耐受性。一个独立数据监测委员会日前按照预定计划对MONALEESA-2进行了中期数据分析发现,ribociclib联合来曲唑和安慰剂对照组(联合来曲唑)相比显著改善这些患者的无进展生存期(PFS)。不良事件与之前报道的结果相似。虽然该试验因伦理原因被终止,对照组患者转移到治疗组,但将继续收集患者的总生存期数据。这个中期临床结果的详细数据会在相关医学会议上报道。
【药源解析】:之前我们多次讨论过,鉴于细胞周期蛋白依赖性激酶(CDK)对正常细胞的调控功能以及制备高选择性CDK抑制剂的技术挑战,CDK抑制剂类的新药开发一直缓慢。直到2009年辉瑞才全速推进其口服、选择性的CDK4/6抑制剂palbociclib的临床开发,并在2015年2月3日获得FDA加速批准上市(商品名:Ibrance),推出临床上首个CDK4/6抑制剂。结果Ibrance获得巨大商业成功,上市当年的销售就高达7.23亿美元。而且Ibrance今年的销售继续高歌猛进,第一季度又给辉瑞带来4.29亿美元收入,迅速进入重磅产品序列。多个机构预测Ibrance的销售峰值将超过45亿美元。
随着Ibrance的商业成功,开发选择性的CDK4/6抑制剂的竞争也变得前所未有的激烈。目前最有希望和辉瑞Ibrance竞争的在研产品有诺华的ribociclib(LEE011)和礼来的abemaciclib。除此之外,G1 Therapeutics的G1T38也针对Ibrance相同的适应症,试图开发所谓的“best-in-class”CDK4/6抑制剂。当然辉瑞的Ibrance至少在HR+/HER2-晚期乳腺癌这个适应症上遥遥领先,并继续巩固其在相关患者人群的领先地位,那么其它“选手”能对Ibrance构成威胁,蚕食一部分的CDK4/6抑制剂市场吗?
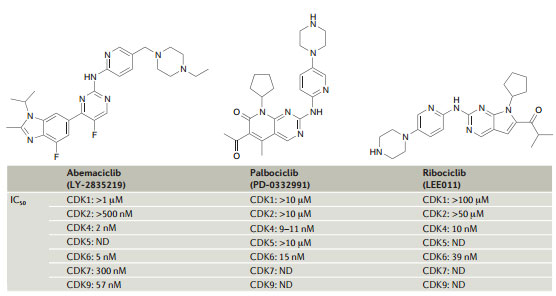
上图是abemaciclib、palbociclib(Ibrance)和ribociclib三个CDK4/6抑制剂的化学结构和体外活性和选择性。从这些初步体外数据来看Ibrance、ribociclib、和abemaciclib的区别不大,礼来的abemaciclib体外活性稍高但在临床上也不应该显示明显区分。事实上到目前为止还未有数据表明ribociclib或abemaciclib在这个人群显示和Ibrance相比的任何疗效或安全性优势。根据一个用于申报的,有165位ER阳性、HER2阴性晚期乳腺癌患者参与的2期临床结果,Ibrance/来曲唑联合治疗组相比来曲唑单药组无进展生存期(PFS)从10.2个月延长至20.2个月,但中期分析显示总生存率并未改善。ribociclib或abemaciclib同样没有总生存期数据。据称礼来的abemaciclib和辉瑞、诺华产品相比潜在的临床区分最大,主要表现在肠胃道副作用相对较小,有望能每天给药,提高CDK4/6抑制剂的临床疗效。而且和其它两个产品相比骨髓抑制也更少。不过这些结果都不具有统计学显著。
虽然诺华ribociclib的3期临床因疗效显著被提前终止,即使马上申报其上市时间也要比辉瑞晚2年,再加上和Ibrance相比未有明显临床区分,除非将来在总生存期方面显示明显优势否则很难对Ibrance的市场销售造成威胁。和诺华相比礼来的abemaciclib情况稍好,但也不大可能蚕食Ibrance现有的较大市场份额。因此,palbociclib的paloma-3实验、ribociclib的MONALEESA-2实验、以及abemaciclib的Monarch2临床结果是这3个CDK4/6双抑制剂在乳腺癌这个适应症领域角逐的关键。
以上开发CDK4/6抑制剂的市场竞争也是以me-too/me-better药物开发为代表的,没有明显临床区分药物开发的一个缩影。随着支付方进一步主宰处方药的使用,这部分产品将进一步受到市场挤压。药源最近报道即使象Opdivo这样的明星产品也会遭到支付方的拒绝(见“NICE拒绝Opdivo,支付政策决定新药产出” )。因此,相同机制或me-too药物的开发要充分利用癌症不是一种疾病这个先天条件,充分利用生物标记和first-in-class产生一些临床区分。比如罗氏的抗PD-L1抗体虽然比Opdivo和Keytruda晚上市2年,但在晚期膀胱癌这个适应症率先上市(见“FDA批准首个PD-L1抗体atezolizumab”)。更重要的是atezolizumab能充分利用罗氏庞大的抗肿瘤产品线和更多的产品开发联合用药。G1 Therapeutics也从降低化疗对骨髓和免疫系统损伤的另一个方面着手,开发其G1T28的不同适应症。当然,因为这是开发全新适应症,虽然CDK4/6抑制剂已经被证实治疗HR+/HER2-晚期乳腺癌有效,但对其它适应症并没有多少指导作用,仍然将面临首创药物的大多数风险。
原文作者:吕顺
原文链接:http://www.yypharm.com/?p=6962,美中药源