-
默沙东肿瘤免疫疗法Keytruda获英国NICE批准
英国国家卫生与临床优化研究所(NICE)近日发布最终治疗指南,批准默沙东(Merck & Co)PD-1肿瘤免疫疗法Keytruda(pembrolizumab)用于英国国家服务系统(NHS),用于既往接受含铂化疗后病情进展的局部晚期或转移性尿路上皮癌(UC)患者的治疗。值得一提的是,此次批准使Keytruda成为进入英国NHS治疗UC的首个也是唯一一个肿瘤免疫疗法。现在,英国的患者可通过癌症药物基金(CDF)获取Keytruda治疗。据估计,在英国每年确诊为尿路上皮癌的患者超过9000
2018-03-30 -
卫材在中国推出治疗功能性消化不良新药Cidine(希笛尼)
日本药企卫材(Eisai)近日宣布其中国子公司卫材中国(总部:江苏省苏州市)在中国市场推出胃肠促动力剂Cidine(酒石酸西尼必利,中文品牌名:希笛尼),该药适用于轻度至中度功能性消化不良的患者,改善早饱、餐后饱胀不适、腹部胀气症状。功能性消化不良是指具有上腹痛、上腹胀、早饱、嗳气、食欲不振、恶心、呕吐等不适症状,经检查排除引起上述症状的器质性疾病的一组临床综合征。在中国,FD患病率约为20%,虽为良性疾病,但常反复发作,病程较长,患者大多四处就医,重复大量检查,不仅耗费医疗资源,给个人和社会均
2018-03-30 -

美国FDA授予强生靶向抗癌药erdafitinib突破性药物资格
美国医药巨头强生(JNJ)近日宣布,美国食品和药物管理局(FDA)已授予靶向抗癌药erdafitinib治疗转移性尿路上皮癌(mUC)的突破性药物资格(BTD)。erdafitinib是一种泛-成纤维细胞生长因子受体(FGFR)酪氨酸激酶抑制剂(TKI),有望成为治疗mUC的首个靶向药物。BTD是FDA在2012年创建的一个新药评审通道,旨在加快开发及审查用于治疗严重或威及生命的疾病并且有初步临床证据表明该药与现有治疗药物相比能够实质性改善病情的新药。获得BTD的药物,在研发时能得到包括FDA高
2018-03-30 -

默沙东抗病毒新药Prevymis获欧盟批准
根据国外医药网站Pharmatimes报道,美国制药巨头默沙东(Merck & Co)抗病毒新药Prevymis(letermovir,MK-8228)片剂和静脉制剂已获欧盟委员会(EC)批准,用于巨细胞病毒(CMV)血清反应阳性的异基因造血干细胞移植(allo-HSCT)成人受者(R+),用于预防CMV的重新激活及感染疾病。在美国,Prevymis已于2017年11月获批,成为美国市场在过去15年来用于预防和治疗CMV感染的首个新药。CMV是allo-HSCT受者中一种常见且潜在严重的
2018-03-30 -
基因泰克兰尼单抗注射液FDA批准用于糖尿病视网膜病变治疗
3月21日,罗氏子公司基因泰克公布称,美国FDA已批准公司Lucentis(ranibizumab-兰尼单抗)0.3mg预填充注射剂(PFS)作为一种新给药剂型用于所有糖尿病视网膜病的治疗。预计将在2018年第二季度上市销售。基因泰克全球产品开发主管、首席医学官Sandra Horning博士表示:“糖尿病视网膜病变是一种严重的疾病,影响着美国数百万人。今天,0.3mg Lucentis预填充注射剂型的批准,加强了我们为那些受这种视力威胁疾病患者提供疗法革新的使命。”2016年10月,Lucen
2018-03-23 -

礼来类风湿关节炎新药baricitinib再次申请上市
近日,礼来公司(Eli Lilly)的类风湿性关节炎(RA)药物baricitinib(商品名Olumiant)重新提交给美国FDA审核,以寻求监管批准(regulatory approval)。2017年2月,baricitinib获批在欧盟国家上市,单独或与甲氨蝶呤(methotrexate)同时使用,作为二线疗法治疗成人患者的严重活跃性类风湿关节炎。但2017年4月,该药物曾因安全性问题而未获FDA批准。类风湿性关节炎(RA)是种自身免疫性疾病,由免疫细胞攻击关节滑膜细胞导致。它是目前最普
2018-03-23 -

FDA授予基因泰克血友病新药emicizumab优先审评资格
罗氏集团(Roche Group)旗下公司基因泰克(Genentech) 今天宣布, FDA已经接受了该公司新药emicizumab的生物制剂许可申请(BLA),并颁发了优先审评资格。该药物是作为对患有产生因子VIII抑制物的A型血友病(hemophilia A)的成年人、青少年和儿童的预防性治疗。2015年9月,FDA已向emicizumab颁发了突破性疗法认定。此次向emicizumab颁发优先审评资格,有望使这款治疗血友病新药早日与患者见面。A型血友病是一种严重的遗传性疾病,病人血液不能正
2017-08-25 -
美国FDA批准DUZALLO用于治疗痛风患者的高尿酸血症
近日,Ironwood Pharmaceuticals宣布美国FDA批准其每日一次口服新药DUZALLO用于治疗痛风患者的高尿酸血症。这些患者单独使用别嘌醇(allopurinol)不能达到目标血清尿酸(sUA)水平。Ironwood预计该药物会于2017年末上市。痛风是由较高的血清尿酸水平导致的一种炎性关节炎,会导致疼痛和严重的长期健康后果。一些患者可以通过使用黄嘌呤氧化酶抑制剂(XOI)——别嘌醇,来降低血清尿酸水平。但在美国,有约200万名在使用XOI治疗的患者的病情无法控制,不能达到美国
2017-08-24 -

FDA批准辉瑞ADC药物Besponsa
今天FDA批准了辉瑞的CD22抗体inotuzumab 与烯二炔毒素ozogamicin 的抗体药物偶联药物(ADC)Besponsa(通用名inotuzumab ozogamicin),用于成人复发难治B细胞ALL。这个批准是根据一个叫做INO-VATE ALL的三期临床结果,326位ALL患者分别使用Besponsa和标准化疗,结果Besponsa组PFS和OS分别为5和7.7个月、化疗组分别为1.8和6.7个月,但OS优势没有达到统计显著。完全应答率Besponsa组明显高于
2017-08-18 -
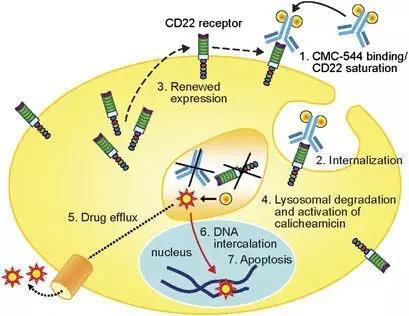
重磅!首款CD22抗体药物偶联物BESPONSA获FDA加速批准
今日,医药行业传来一条重磅新闻——辉瑞(Pfizer)宣布,美国FDA加速批准了其新药BESPONSA(inotuzumab ozogamicin)上市,治疗成人复发或难治性B细胞前体急性淋巴性白血病(B-cell precursor acute lymphoblastic leukemia)。值得一提的是,这是首款获得美国FDA批准的靶向CD22的抗体药物偶联物(ADC)。急性淋巴性白血病是一种侵袭性极高的白血病,在成人患者中的预后极差。据估计,2017年全美大约有5970个新发病例,其中大约
2017-08-18 -
美国FDA批准阿斯利康卵巢癌新款维持疗法
今日,美国FDA宣布批准阿斯利康(AstraZeneca)的Lynparza(olaparib)片剂,用于复发性上皮卵巢癌、输卵管癌、或原发性腹膜癌成人患者的维持治疗。这些患者在先前接受铂类化疗后,正处于完全或部分缓解期。卵巢癌是女性癌症患者最常见的死因之一。在带有BRCA突变等特定遗传性基因异常的情况下,女性发生卵巢癌的风险会显著增加。由阿斯利康研发的olaparib是一款口服聚ADP核糖聚合酶(PARP)抑制剂,可以利用肿瘤DNA损伤反应(DDR)通路缺陷来杀伤癌细胞。2014年,olapa
2017-08-18 -

阿斯利康获FDA授予血液癌症领域首个突破性疗法认定
今日,阿斯利康(AstraZeneca)及其血液学研发卓越中心Acerta Pharma宣布,美国FDA向其在研新药acalabrutinib颁发了突破性疗法认定,用于至少接受过一次治疗的套细胞淋巴瘤(MCL)患者。这也是继PD-L1抑制剂Imfinzi在昨日获得突破性疗法认定后,阿斯利康在本周斩获的第2项突破性疗法认定。值得一提的是,这是阿斯利康在血液癌症的治疗领域收获的首个突破性疗法认定!套细胞淋巴瘤(MCL)是一种高侵袭性的B细胞非霍奇金淋巴瘤(NHL),患者预后很差。治疗这种恶性疾病,也
2017-08-02 -
重磅免疫疗法Opdivo获美国FDA加速批准用于直肠癌
今日,百时美施贵宝(Bristol-Myers Squibb)宣布,其重磅免疫疗法Opdivo(nivolumab)得到了美国FDA的加速批准,用于治疗微卫星不稳定性高(MSI-H)或错配修复缺陷(dMMR)的转移性结直肠癌患者。结直肠癌是病发于结肠或直肠的癌症。在美国,它是第三常见的癌症,预计在2017年会增加13.5万个新病例。值得注意的是,它也是美国致死率第二高的癌症。在这些患者中,大约有5%的患者带有MSI-H与dMMR这两种常见的遗传异常。含有这两种变异的肿瘤,细胞内的DNA修复机制往
2017-08-02 -

FDA批准急性髓系白血病新药enasidenib上市
FDA 8月1日批准新基公司Idhifa (enasidenib)上市,用于治疗携带异柠檬酸脱氢酶2(IDH2)基因突变的成人复发或难治性急性髓系白血病。FDA同时批准了雅培的RealTime IDH2 Assay伴随诊断试剂盒。Enasidenib属于first in class的异柠檬酸脱氢酶2抑制剂,可以抑制多种促进细胞增殖的酶的活性。如果患者血液或骨髓样本中检测到了IDH2突变,便适用于接受enasidenib治疗。AML患者中携带IDH2突变的比例大约为8%~19%。AML是一种快速进
2017-08-02 -

FDA批准首款致癌代谢物合成抑制剂enasidenib
【新闻事件】:今天FDA批准了新基和Agios的变异IDH2抑制剂enasidenib (商品名Idhifa,曾用名AG-221)用于治疗IDH2变异、复发难治型AML,同时批准了雅培的RealTime IDH2检验试剂盒。这个决定是根据一个199人参与的一/二期单臂临床试验结果,使用6个月以上Idhifa有19%病人完全应答。中值应答时间为8.2个月,完全应答人群中值生存期为19.7个月。34%用药前需要输血的病人用药后可以避免输血,但77%患者也出现白血球增多、维甲酸综合症等严重副反应。ID
2017-08-02 -
礼来 /Incyte 巴瑞克替尼在日本获批用于类风湿性关节炎
7 月 3 日,美国礼来制药公司同 Incyte 制药公司表示,日本厚生劳动省(MHLW)批准了公司 2mg 及 4mg 的 Olumiant? (baricitinib,巴瑞克替尼) 片剂用于对现有标准疗法响应不佳的类风湿性关节炎(包括对关节结构损伤的预防)患者的治疗。Olumiant 的批准是基于 baricitinib 的临床开发项目,包括 4 项临床 III 期研究,在全球范围共招募了 3000 名各种类型的中重度类风湿性关节炎的患者(包括 500 名日本地区患者)。结果显示,相比标准疗
2017-07-05

